لاصقة الإنسولين الذكية لعلاج داء السكري
بلكي الإخباري يعتبر مرض السكري واحدًا من أكبر التحديات الطبية في القرن الواحد والعشرين، حيث يعاني منه أكثر من 280 مليون شخص على مستوى العالم1. ويجب على كل من هؤلاء مراقبة مستويات السكر في الدم لديهم، وحقن الجرعة الصحيحة من هرمون الإنسولين الخافض للجلوكوز؛ للحفاظ على مستويات السكر في معدلها الطبيعي2، لكن طريقة المعالجة تلك تشمل العديد من التحديات، فهي تتطلب حَقْنًا مؤلمًا ومزعجًا تحت الجلد، إضافة إلى أنها غير دقيقة، ويمكن أن تسبب مشكلات خطيرة، إذا لم يتم ضبط جرعة الإنسولين، حسب الاحتياجات الفسيولوجية الضرورية للمريض3. فقد قام يو وزملاؤه4 في بحثهم المنشور في دورية "أعمال الأكاديمية الوطنية للعلوم" بوصف لاصقة تحتوي على إبرة مجهرية تستجيب للجلوكوز، يمكن وضعها ـ من دون ألم ـ على الجلد؛ فتطلق الإنسولين عند ارتفاع مستويات السكر في الدم.
إن العلاجات "الذكية" المعتمدة على الإنسولين تعتمد على الإفراج التلقائي للهرمون، استجابةً للزيادة في نِسَب السكر في الدم، ويمكنها أن تحسِّن التحكم في المرض، والحدّ من احتمالات انخفاض مستويات الجلوكوز بشكل مفرط، وهو التأثير القاتل لجرعات الإنسولين الزائدة3. ولإشباع الاحتياجات الفسيولوجية للمريض، يجب على مثل هذه العلاجات أن تستجيب بسرعة لمستويات الجلوكوز المرتفعة، وأن تُطْلِق الإنسولين بحركة تماثل ما يحدث في البنكرياس السليم.
يَستخدم أحد هذه العلاجات الذكية نُظُمًا لإيصال الإنسولين، يتم التحكم فيها عن طريق حاسب آلي صغير، حيث يوصل تلك النظم مراقب مستمر لمستوى الجلوكوز (CGMS)، قابل للزراعة في الجسم بمضخات آلية، تُطْلِق الإنسولين عن طريق إبرة حقن مزروعة تحت الجلد. ويجري حاليًا تقييم هذه الأجهزة إكلينيكيًّا، حيث أظهرت نتائج إيجابية في مساعدة المرضى على ضبط مستوى السكر لديهم بشكل أكثر انتظامًا5,6، إلا أن أجهزة استشعار المراقب المستخدَم حاليًا تحتاج معايرة عدة مرات في اليوم باستخدام جهاز محمول لقياس الجلوكوز، يعطي قياسات متأخرة بـ5-15 دقيقة، مما يعرقل جهود الحفاظ على المستويات الطبيعية3. كما أن حجمها يماثل حجم جهاز الاستدعاء الصغير، وتزيد أجهزة الاستشعار وإبرة الحقن من خطر الإصابة بالالتهابات، كما تتطلب صيانة متكررة واستبدالات لمكافحة استجابة المناعة في الجسم، مما يقلل من راحة المريض، ويزيد التكلفة التي يتحملها3.
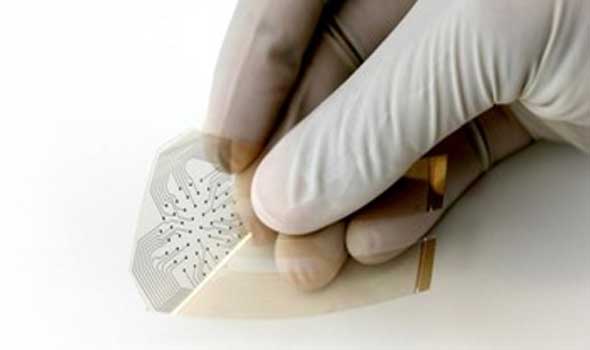
إن جهاز لاصقة الإِبَر المجهرية ـ الذي طوّره يو وزملاؤه ـ هو بمثابة نظام مكوَّن من 121 إبرة مخروطية في مساحة 6 ملِّيمترات مربعة، يبلغ قطر كل واحدة منها 300 ميكرومتر عند القاعدة، و10 عند القمة، ويبلغ ارتفاعها 600 ميكرومتر. تحتوي الإبر على جسيمات نانوية، مصمَّمة من قِبَل المؤلفين، تتكون من ثلاثة عناصر: الإنسولين، وإنزيم الجلوكوز أوكسيديز (الذي يستهلك الأكسجين؛ ليحوِّل الجلوكوز إلى حمض الجلوكونيك)، وبوليمر محيط يتفكك في البيئات منخفضة الأكسجين. في هذا النظام، يعمل الجلوكوز أوكسيديز كجهاز استشعار للجلوكوز، بينما يعمل البوليمر كمحرِّك لإفراز الإنسولين.
وعندما يتم وضع اللاصقة، تغطس الإبر المجهرية في السائل الموجود بين الخلايا تحت الجلد. وتُعَدّ نظرية العمل على النحو التالي: مع ارتفاع مستويات السكر في الدم، يزداد النشاط الإنزيمي للجلوكوز أوكسيديز، مما يؤدي إلى خلق بيئة خالية من الأكسجين داخل الجسيمات النانوية، مما يتسبب في تفكك الجسيمات النانوية، وإطلاق الإنسولين (الشكل 1). وباستخدام هذا النهج الكيميائي، يأمل المؤلفون إلى الوصول إلى أوقات استجابة سريعة، وحركة إطلاق للإنسولين، مِن شأنها أن تلبِّي ـ على نحو أفضل ـ حاجة المريض إلى الإنسولين.
لاصقة الإِبَر المجهرية، لمراقبة مستويات الجلوكوز، وإفراز الإنسولين.
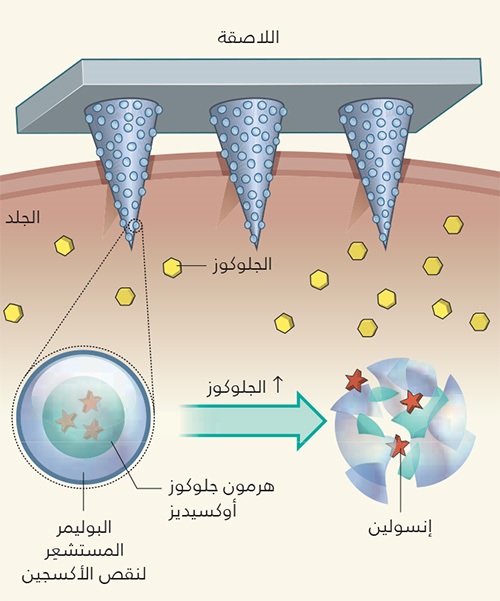 صَمَّم يو وزملاؤه4 لاصقة ذكية لإفراز الإنسولين، مصنوعة من 121 إبرة مجهرية، تحتوي على جسيمات نانوية. تخترق اللاصقة السائل الموجود بين الخلايا تحت الجلد، من دون ألم. وتحتوي الجسيمات النانوية في كل إبرة على الإنسولين، وإنزيم الجلوكوز أوكسيديز المستشعِر للجلوكوز، الذي يحوِّل الجلوكوز إلى حمض الجلوكونيك، كما تحاط هذه الجزيئات بالبوليمر المستشعِر لنقص الأكسجين. يؤدي ارتفاع تركيز الجلوكوز إلى زيادة نشاط الجلوكوز أوكسيديز، الأمر الذي يؤدي بدوره إلى خَلْق بيئة منخفضة الأكسجين في الجسيمات النانوية، التي يستشعرها البوليمر؛ مما يؤدي إلى تفككها، وإطلاق الإنسولين.
أثبت يو وزملاؤه أن هذه اللاصقات تُطلق الإنسولين بطريقة ذكية تستجيب لتركيز الجلوكوز، مع آلية عمل يمكن تعديلها عن طريق تغيير تركيز هرمون الجلوكوز أوكسيديز المحمَّل على الإبر المجهرية. ووجد الباحثون في تجارب على الجسم الحي ـ باستخدام فئران تعاني من مرض السكري ـ أن اللاصقة الواحدة يمكن أن تنظم مستويات السكر في الدم على نحو فعال، كما أنه عندما أُعطيت الحيوانات جرعات زائدة من الجلوكوز، استجابت اللاصقة على النحو المتوقع، حيث أطلقت الإنسولين، وخفضت مستويات الجلوكوز إلى المستوى الطبيعي. والأهم من ذلك.. أنه بمجرد الوصول إلى المستويات الطبيعية، توقفت اللاصقة عن إطلاق الإنسولين، مما يقلل المخاطر المحتملة من الانخفاض المفرط للجلوكوز. وأخيرًا، من خلال الاستعمال المتكرر للاصقات، توصَّل المؤلفون إلى تصحيح طويل الأمد لتركيز الجلوكوز في الفئران المصابة بالسكري.
وتُعتبر اللاصقات ذات الإبر المجهرية بديلًا جذابًا لأي علاج يعتمد على الحقن7. يَدرِس الباحثون حاليًّا إمكانية استخدام مثل تلك اللاصقات؛ لإعطاء التطعيمات، وللعلاج الجيني، ولتقديم الهرمونات الأخرى التي تتطلب أن يتم تناولها بانتظام، لكن الابتكار في عمل يو وزملائه يكمن في القدرة على إفراز الإنسولين من الإِبَر المجهرية بطريقة تعتمد على تركيز الجلوكوز في الدم. ولذلك.. فهناك حاجة إلى إتمام التجارب على الحيوانات الأكبر، وتحليلات أكثر تفصيلًا حول حركة إطلاق الإنسولين باستخدام هذه التقنية، لتحديد مدى جدوى استخدام هذه الطريقة إكلينيكيًّا. وقبل أن يتمكن المرضى من استخدام اللاصقات، سيكون من الضروري تقييم التفاعلات المناعية المحتملة، التي قد تحدث ردًّا على التعرض المتكرر لمختلف مكونات هذه اللاصقات. ومع ذلك.. تقدم تلك التقنية طريقة واعدة لتطوير نظم إطلاق الإنسولين، اعتمادًا على تركيز الجلوكوز.
وبما أنه لا يوجد حاليًّا أي علاج لمرض السكري، فإن تقنيات مثل التي يقدمها يو وزملاؤه تُعتبر ضرورية، حيث تساعِد مرضى السكري على التحكم بأعراض مرضهم بشكل أكثر أمانًا وسهولة. كما أن هناك طرقًا أخرى قيد البحث، تعتمد على استبدال أو تجديد خلايا بيتا في البنكرياس، التي تستجيب للجلوكوز، وتفرز الإنسولين للحفاظ على مستويات السكر الطبيعية في الدم8. وتبشر هذه الاستراتيجيات بشفاء كامل من مرض السكري. وقد تم إحراز تقدُّم كبير في عملية استبدال خلايا بيتا، والتقنيات التي من شأنها أن تمكِّن زَرْعها بشكل آمِن وفعّال في المرضى. وعلى الرغم من هذا التقدم، ما زال الشفاء بعيد المنال، وربما يحتاج إلى سنوات. وفي غضون ذلك.. مِن المؤكد أن المرضى سيرحِّبون بوسيلة آمِنة وفعّالة وغير مؤلمة؛ للتحكم في مرضهم.
صَمَّم يو وزملاؤه4 لاصقة ذكية لإفراز الإنسولين، مصنوعة من 121 إبرة مجهرية، تحتوي على جسيمات نانوية. تخترق اللاصقة السائل الموجود بين الخلايا تحت الجلد، من دون ألم. وتحتوي الجسيمات النانوية في كل إبرة على الإنسولين، وإنزيم الجلوكوز أوكسيديز المستشعِر للجلوكوز، الذي يحوِّل الجلوكوز إلى حمض الجلوكونيك، كما تحاط هذه الجزيئات بالبوليمر المستشعِر لنقص الأكسجين. يؤدي ارتفاع تركيز الجلوكوز إلى زيادة نشاط الجلوكوز أوكسيديز، الأمر الذي يؤدي بدوره إلى خَلْق بيئة منخفضة الأكسجين في الجسيمات النانوية، التي يستشعرها البوليمر؛ مما يؤدي إلى تفككها، وإطلاق الإنسولين.
أثبت يو وزملاؤه أن هذه اللاصقات تُطلق الإنسولين بطريقة ذكية تستجيب لتركيز الجلوكوز، مع آلية عمل يمكن تعديلها عن طريق تغيير تركيز هرمون الجلوكوز أوكسيديز المحمَّل على الإبر المجهرية. ووجد الباحثون في تجارب على الجسم الحي ـ باستخدام فئران تعاني من مرض السكري ـ أن اللاصقة الواحدة يمكن أن تنظم مستويات السكر في الدم على نحو فعال، كما أنه عندما أُعطيت الحيوانات جرعات زائدة من الجلوكوز، استجابت اللاصقة على النحو المتوقع، حيث أطلقت الإنسولين، وخفضت مستويات الجلوكوز إلى المستوى الطبيعي. والأهم من ذلك.. أنه بمجرد الوصول إلى المستويات الطبيعية، توقفت اللاصقة عن إطلاق الإنسولين، مما يقلل المخاطر المحتملة من الانخفاض المفرط للجلوكوز. وأخيرًا، من خلال الاستعمال المتكرر للاصقات، توصَّل المؤلفون إلى تصحيح طويل الأمد لتركيز الجلوكوز في الفئران المصابة بالسكري.
وتُعتبر اللاصقات ذات الإبر المجهرية بديلًا جذابًا لأي علاج يعتمد على الحقن7. يَدرِس الباحثون حاليًّا إمكانية استخدام مثل تلك اللاصقات؛ لإعطاء التطعيمات، وللعلاج الجيني، ولتقديم الهرمونات الأخرى التي تتطلب أن يتم تناولها بانتظام، لكن الابتكار في عمل يو وزملائه يكمن في القدرة على إفراز الإنسولين من الإِبَر المجهرية بطريقة تعتمد على تركيز الجلوكوز في الدم. ولذلك.. فهناك حاجة إلى إتمام التجارب على الحيوانات الأكبر، وتحليلات أكثر تفصيلًا حول حركة إطلاق الإنسولين باستخدام هذه التقنية، لتحديد مدى جدوى استخدام هذه الطريقة إكلينيكيًّا. وقبل أن يتمكن المرضى من استخدام اللاصقات، سيكون من الضروري تقييم التفاعلات المناعية المحتملة، التي قد تحدث ردًّا على التعرض المتكرر لمختلف مكونات هذه اللاصقات. ومع ذلك.. تقدم تلك التقنية طريقة واعدة لتطوير نظم إطلاق الإنسولين، اعتمادًا على تركيز الجلوكوز.
وبما أنه لا يوجد حاليًّا أي علاج لمرض السكري، فإن تقنيات مثل التي يقدمها يو وزملاؤه تُعتبر ضرورية، حيث تساعِد مرضى السكري على التحكم بأعراض مرضهم بشكل أكثر أمانًا وسهولة. كما أن هناك طرقًا أخرى قيد البحث، تعتمد على استبدال أو تجديد خلايا بيتا في البنكرياس، التي تستجيب للجلوكوز، وتفرز الإنسولين للحفاظ على مستويات السكر الطبيعية في الدم8. وتبشر هذه الاستراتيجيات بشفاء كامل من مرض السكري. وقد تم إحراز تقدُّم كبير في عملية استبدال خلايا بيتا، والتقنيات التي من شأنها أن تمكِّن زَرْعها بشكل آمِن وفعّال في المرضى. وعلى الرغم من هذا التقدم، ما زال الشفاء بعيد المنال، وربما يحتاج إلى سنوات. وفي غضون ذلك.. مِن المؤكد أن المرضى سيرحِّبون بوسيلة آمِنة وفعّالة وغير مؤلمة؛ للتحكم في مرضهم.
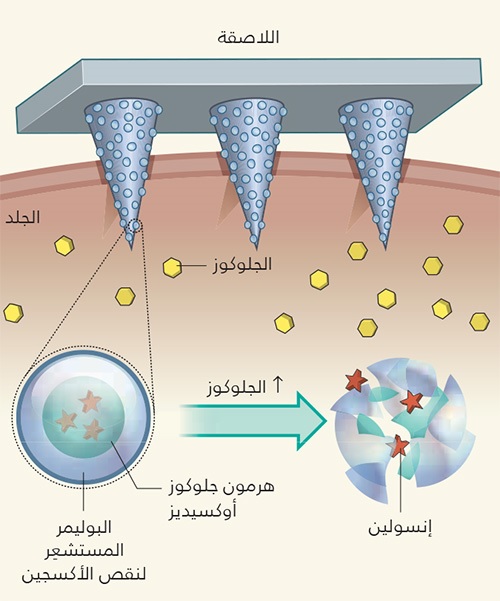
 صَمَّم يو وزملاؤه4 لاصقة ذكية لإفراز الإنسولين، مصنوعة من 121 إبرة مجهرية، تحتوي على جسيمات نانوية. تخترق اللاصقة السائل الموجود بين الخلايا تحت الجلد، من دون ألم. وتحتوي الجسيمات النانوية في كل إبرة على الإنسولين، وإنزيم الجلوكوز أوكسيديز المستشعِر للجلوكوز، الذي يحوِّل الجلوكوز إلى حمض الجلوكونيك، كما تحاط هذه الجزيئات بالبوليمر المستشعِر لنقص الأكسجين. يؤدي ارتفاع تركيز الجلوكوز إلى زيادة نشاط الجلوكوز أوكسيديز، الأمر الذي يؤدي بدوره إلى خَلْق بيئة منخفضة الأكسجين في الجسيمات النانوية، التي يستشعرها البوليمر؛ مما يؤدي إلى تفككها، وإطلاق الإنسولين.
أثبت يو وزملاؤه أن هذه اللاصقات تُطلق الإنسولين بطريقة ذكية تستجيب لتركيز الجلوكوز، مع آلية عمل يمكن تعديلها عن طريق تغيير تركيز هرمون الجلوكوز أوكسيديز المحمَّل على الإبر المجهرية. ووجد الباحثون في تجارب على الجسم الحي ـ باستخدام فئران تعاني من مرض السكري ـ أن اللاصقة الواحدة يمكن أن تنظم مستويات السكر في الدم على نحو فعال، كما أنه عندما أُعطيت الحيوانات جرعات زائدة من الجلوكوز، استجابت اللاصقة على النحو المتوقع، حيث أطلقت الإنسولين، وخفضت مستويات الجلوكوز إلى المستوى الطبيعي. والأهم من ذلك.. أنه بمجرد الوصول إلى المستويات الطبيعية، توقفت اللاصقة عن إطلاق الإنسولين، مما يقلل المخاطر المحتملة من الانخفاض المفرط للجلوكوز. وأخيرًا، من خلال الاستعمال المتكرر للاصقات، توصَّل المؤلفون إلى تصحيح طويل الأمد لتركيز الجلوكوز في الفئران المصابة بالسكري.
وتُعتبر اللاصقات ذات الإبر المجهرية بديلًا جذابًا لأي علاج يعتمد على الحقن7. يَدرِس الباحثون حاليًّا إمكانية استخدام مثل تلك اللاصقات؛ لإعطاء التطعيمات، وللعلاج الجيني، ولتقديم الهرمونات الأخرى التي تتطلب أن يتم تناولها بانتظام، لكن الابتكار في عمل يو وزملائه يكمن في القدرة على إفراز الإنسولين من الإِبَر المجهرية بطريقة تعتمد على تركيز الجلوكوز في الدم. ولذلك.. فهناك حاجة إلى إتمام التجارب على الحيوانات الأكبر، وتحليلات أكثر تفصيلًا حول حركة إطلاق الإنسولين باستخدام هذه التقنية، لتحديد مدى جدوى استخدام هذه الطريقة إكلينيكيًّا. وقبل أن يتمكن المرضى من استخدام اللاصقات، سيكون من الضروري تقييم التفاعلات المناعية المحتملة، التي قد تحدث ردًّا على التعرض المتكرر لمختلف مكونات هذه اللاصقات. ومع ذلك.. تقدم تلك التقنية طريقة واعدة لتطوير نظم إطلاق الإنسولين، اعتمادًا على تركيز الجلوكوز.
وبما أنه لا يوجد حاليًّا أي علاج لمرض السكري، فإن تقنيات مثل التي يقدمها يو وزملاؤه تُعتبر ضرورية، حيث تساعِد مرضى السكري على التحكم بأعراض مرضهم بشكل أكثر أمانًا وسهولة. كما أن هناك طرقًا أخرى قيد البحث، تعتمد على استبدال أو تجديد خلايا بيتا في البنكرياس، التي تستجيب للجلوكوز، وتفرز الإنسولين للحفاظ على مستويات السكر الطبيعية في الدم8. وتبشر هذه الاستراتيجيات بشفاء كامل من مرض السكري. وقد تم إحراز تقدُّم كبير في عملية استبدال خلايا بيتا، والتقنيات التي من شأنها أن تمكِّن زَرْعها بشكل آمِن وفعّال في المرضى. وعلى الرغم من هذا التقدم، ما زال الشفاء بعيد المنال، وربما يحتاج إلى سنوات. وفي غضون ذلك.. مِن المؤكد أن المرضى سيرحِّبون بوسيلة آمِنة وفعّالة وغير مؤلمة؛ للتحكم في مرضهم.
صَمَّم يو وزملاؤه4 لاصقة ذكية لإفراز الإنسولين، مصنوعة من 121 إبرة مجهرية، تحتوي على جسيمات نانوية. تخترق اللاصقة السائل الموجود بين الخلايا تحت الجلد، من دون ألم. وتحتوي الجسيمات النانوية في كل إبرة على الإنسولين، وإنزيم الجلوكوز أوكسيديز المستشعِر للجلوكوز، الذي يحوِّل الجلوكوز إلى حمض الجلوكونيك، كما تحاط هذه الجزيئات بالبوليمر المستشعِر لنقص الأكسجين. يؤدي ارتفاع تركيز الجلوكوز إلى زيادة نشاط الجلوكوز أوكسيديز، الأمر الذي يؤدي بدوره إلى خَلْق بيئة منخفضة الأكسجين في الجسيمات النانوية، التي يستشعرها البوليمر؛ مما يؤدي إلى تفككها، وإطلاق الإنسولين.
أثبت يو وزملاؤه أن هذه اللاصقات تُطلق الإنسولين بطريقة ذكية تستجيب لتركيز الجلوكوز، مع آلية عمل يمكن تعديلها عن طريق تغيير تركيز هرمون الجلوكوز أوكسيديز المحمَّل على الإبر المجهرية. ووجد الباحثون في تجارب على الجسم الحي ـ باستخدام فئران تعاني من مرض السكري ـ أن اللاصقة الواحدة يمكن أن تنظم مستويات السكر في الدم على نحو فعال، كما أنه عندما أُعطيت الحيوانات جرعات زائدة من الجلوكوز، استجابت اللاصقة على النحو المتوقع، حيث أطلقت الإنسولين، وخفضت مستويات الجلوكوز إلى المستوى الطبيعي. والأهم من ذلك.. أنه بمجرد الوصول إلى المستويات الطبيعية، توقفت اللاصقة عن إطلاق الإنسولين، مما يقلل المخاطر المحتملة من الانخفاض المفرط للجلوكوز. وأخيرًا، من خلال الاستعمال المتكرر للاصقات، توصَّل المؤلفون إلى تصحيح طويل الأمد لتركيز الجلوكوز في الفئران المصابة بالسكري.
وتُعتبر اللاصقات ذات الإبر المجهرية بديلًا جذابًا لأي علاج يعتمد على الحقن7. يَدرِس الباحثون حاليًّا إمكانية استخدام مثل تلك اللاصقات؛ لإعطاء التطعيمات، وللعلاج الجيني، ولتقديم الهرمونات الأخرى التي تتطلب أن يتم تناولها بانتظام، لكن الابتكار في عمل يو وزملائه يكمن في القدرة على إفراز الإنسولين من الإِبَر المجهرية بطريقة تعتمد على تركيز الجلوكوز في الدم. ولذلك.. فهناك حاجة إلى إتمام التجارب على الحيوانات الأكبر، وتحليلات أكثر تفصيلًا حول حركة إطلاق الإنسولين باستخدام هذه التقنية، لتحديد مدى جدوى استخدام هذه الطريقة إكلينيكيًّا. وقبل أن يتمكن المرضى من استخدام اللاصقات، سيكون من الضروري تقييم التفاعلات المناعية المحتملة، التي قد تحدث ردًّا على التعرض المتكرر لمختلف مكونات هذه اللاصقات. ومع ذلك.. تقدم تلك التقنية طريقة واعدة لتطوير نظم إطلاق الإنسولين، اعتمادًا على تركيز الجلوكوز.
وبما أنه لا يوجد حاليًّا أي علاج لمرض السكري، فإن تقنيات مثل التي يقدمها يو وزملاؤه تُعتبر ضرورية، حيث تساعِد مرضى السكري على التحكم بأعراض مرضهم بشكل أكثر أمانًا وسهولة. كما أن هناك طرقًا أخرى قيد البحث، تعتمد على استبدال أو تجديد خلايا بيتا في البنكرياس، التي تستجيب للجلوكوز، وتفرز الإنسولين للحفاظ على مستويات السكر الطبيعية في الدم8. وتبشر هذه الاستراتيجيات بشفاء كامل من مرض السكري. وقد تم إحراز تقدُّم كبير في عملية استبدال خلايا بيتا، والتقنيات التي من شأنها أن تمكِّن زَرْعها بشكل آمِن وفعّال في المرضى. وعلى الرغم من هذا التقدم، ما زال الشفاء بعيد المنال، وربما يحتاج إلى سنوات. وفي غضون ذلك.. مِن المؤكد أن المرضى سيرحِّبون بوسيلة آمِنة وفعّالة وغير مؤلمة؛ للتحكم في مرضهم.